domingo, 27 de março de 2011
Transferência de energia
Mecanismos ou processos de tranferência de energia sob a forma de calor (condução térmica-sólidos, não há transporte da matéria; convecção térmica-líquidos e sólidos, há transporte da matéria).
Mecanismos
- sólido condução térmica - a energia é transferida de partícula a partícula; não há deslocamento (transporte) da matéria
- líquidos e gases: convecção térmica - há transferência de energia com deslocamento (transporte) da matéria

- líquidos e gases: convecção térmica - há transferência de energia com deslocamento (transporte) da matéria
Calor
É a transferência de energia térmica de 2 corpos em contacto a diferentes temperaturas. Diz-se, também, que calor é energia em trânsito; flui de um corpo a temperatura mais alta para outra a temperatura mais baixa.

Temperatura
Temperatura: é uma grandeza física, que se relaciona como o grau de agitação dos corpúsculos e com a energia cinética média dos corpúsculos. A temperatura mede-se com um termómetro.


ENERGIA
Difícil de definir!;
- A energia transforma-se;
-energia potencial gravítica (Epg=m.g.h. - h-altura, p-peso, m-massa, g-aceleração gravítica),
-energia mecânica,
-energia eléctrica,
-energia radiante,
-energia térmica,
-energia cinética (associada ao movimento);
- A energia cinética e a energia potencial são as 2 formas fundamentais de energia.
- É uma grandeza física não vectorial;
- Não é uma substância, mas também não é uma força- A energia transforma-se;
- Existem várias fontes de energia:
-renováveis (sol, água, vento, biomassa)
-não-renováveis (combustíveis fósseis-petróleo, carvão, gás natural; combustíveis nucleares-uranio, plutónio, ...);
- A energia manifesta-se sob diferentes formas
-não-renováveis (combustíveis fósseis-petróleo, carvão, gás natural; combustíveis nucleares-uranio, plutónio, ...);
- A energia manifesta-se sob diferentes formas
-energia luminosa (luz visível),
-energia potencial elástica,
-energia potencial química,-energia potencial gravítica (Epg=m.g.h. - h-altura, p-peso, m-massa, g-aceleração gravítica),
-energia mecânica,
-energia eléctrica,
-energia radiante,
-energia térmica,
-energia cinética (associada ao movimento);
- A energia cinética e a energia potencial são as 2 formas fundamentais de energia.
Catalisadores
Catalisador é toda e qualquer substâncias que acelera uma reacção, diminuindo a energia de activação, diminuindo a energia do complexo activado, sem ser consumido, durante o processo. Um catalisador normalmente promove um caminho (mecanismo) molecular diferente para a reação.
Velocidade das reacções quimicas
Dá-se um rearranjo dos átomos das substâncias iniciais de forma a obter-se novas substâncias (colisões eficazes entre as moléculas).
Factores:
-Temperatura
T sobe v sobe
-Concentração
C sobe v sobe
-Estado de Divisão do Sólido
Área de Contacto sobe v sobe
Teoria Cinético Corpúscular
- toda a matéria é constituída por corpúsculos;
- a matéria é descontínua, pois existe espaços vazios entre os corpúsculos;
- os corpúsculos encontram-se em constante movimento;
- aumentando a temperatura, a rapidez dos movimentos dos corpúsculos aumenta.
- a matéria é descontínua, pois existe espaços vazios entre os corpúsculos;
- os corpúsculos encontram-se em constante movimento;
- aumentando a temperatura, a rapidez dos movimentos dos corpúsculos aumenta.
Compostos Iónicos e Iões
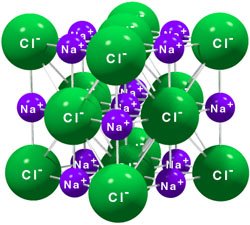
Compostos Iónicos - são substâncias constituídas por iões positivos ( catiões) e por iões negativos ( aniões), o composto iónico sólido é sempre neutro.
Iões - são partículas com carga eléctrica, formados por átomos ( ou conjunto de átomos) que receberam ou perderam eléctrões.
Exemplo:
Atomo de sódio-
Iões - são partículas com carga eléctrica, formados por átomos ( ou conjunto de átomos) que receberam ou perderam eléctrões.
Exemplo:
Atomo de sódio-
Na + 1 electrão (e)+ -----» Na+ -----» ião sódio ----» ião positivo ou catião.

Acerto das equações quimicas
_CH4 (g) +_O2 (g) ---------» _CO2 (g) +_H2O (g)
1C, 4H, 2O, 1C, 2H, 3O
_CH4 (g) + 2O2 (g) ---------» _CO2 (g) + 2H2O (g)
1C, 4H, 4O, 1C, 4H, 4O
Lei de Lavoisier
De acordo com a Lei de Lavoisier , numa reacção quimica, a massa total dos reagentes e igual a massa total dos produtos de reacção num sistema fechado.
"Na Natureza nada se perde, nada se cria, tudo se transforma".
"Na Natureza nada se perde, nada se cria, tudo se transforma".
Formula quimica
Fórmula Química de uma substância molecular (substâncias constituídas por moléculas)
Informação qualitativa: que elementos constituem a molécula
Informação quantitativa: quantos átomos de cada elemento químico
Ex.: a água é uma molécula constituída por 2 átomos de hidrogénio e 1 átomo de oxigénio
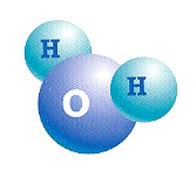
1ºescrevemos o simbolo quimico do elemento quimico
2ºescrevemos a quantidade de atomos do 1º elemento quimico referido (em indice)
3ºdepois continuamos com o que e indicado
Informação qualitativa: que elementos constituem a molécula
Informação quantitativa: quantos átomos de cada elemento químico
Ex.: a água é uma molécula constituída por 2 átomos de hidrogénio e 1 átomo de oxigénio
1ºescrevemos o simbolo quimico do elemento quimico
2ºescrevemos a quantidade de atomos do 1º elemento quimico referido (em indice)
3ºdepois continuamos com o que e indicado
Subscrever:
Mensagens (Atom)

